News & Message
以愛傳承,延續生命 淺談器官移植治療用藥
撰文/中國醫藥大學附設醫院 藥劑部 游逸群藥師
近來電視劇「生死接線員」引發不少探討熱議,除了讓大眾認識醫院裡重要但少為人知的器捐協調師的角色,也重新喚起對器官捐贈的關注。器官移植對於末期器官衰竭的病人而言,確是生命延續的曙光。但器官移植僅能視為一種治療手段,而非治癒疾病的方法,從術前術後的評估,到器官置換後所帶來的好處與長期免疫抑制劑所造成的風險都是並存的。因此,並非所有器官衰竭的病人都適合接受器官移植。
.jpg)
一旦移植接受者評估合適,器官移植手術後首要面對的即是移植後的排斥狀況。以心臟移植為例,術後第一年平均可能發生2~3次的排斥狀況,約有50~80%的心臟移植患者會經歷至少一次的心臟排斥狀況;並有統計發現高達21~30%的心臟移植病患於術後一年會因急性排斥須接受治療。心臟移植後的排斥,依病理切片分類可分為:急性細胞免疫性排斥、抗體免疫性排斥;若依排斥發生時間分類,則可以分為超急性排斥、急性排斥、慢性排斥。一般長期服用的免疫抑制藥物是依據每位移植患者的狀況、肝腎功能與歷次移植物的功能結果來調整。
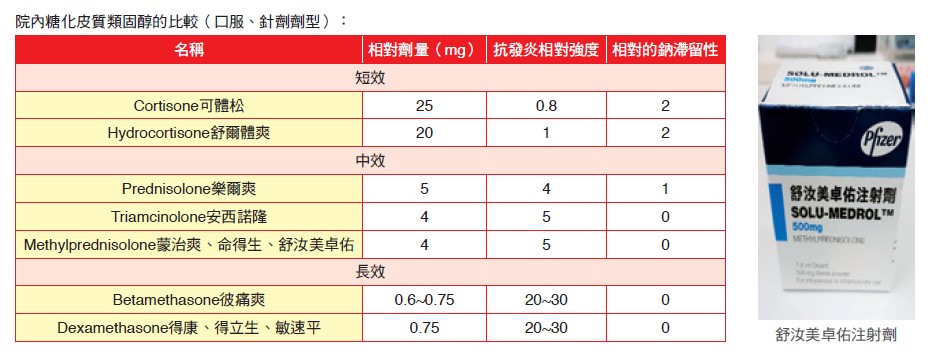
類固醇(Corticosteroids)
類固醇同時具有免疫抑制與抗發炎的特性,作用機轉有抑制細胞激素的轉錄、誘導淋巴球凋亡、降低黏合分子與人類主要組織相容性複合體的表現、改變白血球的的運輸方式。類固醇的副作用與用量多少及使用時間長短有關,發生類型多廣為所知,這裡並不贅述,然用量越大,使用時間越久,副作用出現機率越高。因此在患者接受移植後,會迅速減量至0.1 mg/kg或更低濃度的維持劑量,以降低相關死亡發生率。然而移植後若發生超急性或急性排斥反應,高劑量靜脈注射類固醇則仍是第一線治療方式。
抗增生藥物
1.Calcineurin Inhibitors(CNI):
Cyclosporine(新體睦╱因睦寧軟膠囊)、Tacrolimus(普樂可復膠囊╱安瑞福持續性藥效膠囊)。
Calcineurin抑制劑和細胞內的蛋白immunophilin結合後,抑制calcineurin的磷酸酶的功能,進而抑制T細胞的活化與增生。因會引發腎臟入球小動脈收縮而產生的腎毒性,導致腎絲球濾過率(GFR)立即下降30%,以及造成長期血管阻塞性纖維化腎病的關係,使此類藥物目前在器官移植上多為減量或避免使用。急性腎毒性常是可逆的,但慢性腎毒性一般不可逆,幾乎發生在所有移植術後接受此藥物治療達8-10年的患者身上。
Cyclosporine其他的副作用還包含牙齦增生、多毛症、高血壓、高血脂、葡萄糖不耐症,並極少數發生的血栓性小血管病變。Cyclosporine的治療區間狹窄,劑量建議須根據血液濃度做調整(建議維持最低濃度100-300 ng/mL及2小時濃度<800~1200 ng/mL);通常劑量是6-8 mg/kg/day,分次給予並小心留意藥物濃度及其毒性。
Tacrolimus一樣具有腎毒性,比起Cyclosporine更具有神經毒性與葡萄糖不耐症,但對於如多毛症、牙齦增生、高血壓等副作用則較少見。Tacrolimus的劑量亦根據血中最低濃度來調整(建議維持濃度5-10 ng/mL);通常起始劑量為0.15 mg/kg/day,分次給予。
此類藥物都是由細胞色素P450(3A4)代謝,因此使用上須留意與其他藥物的交互作用。
2. Mammalian Target of Rapamycin(mTOR)Inhibitors:
Sirolimus(斥消靈錠)與Everolimus(卓定康錠)。
此類藥品抑制mammalian target of rapamycin(mTOR)在和FK-binding protein結合以後,可以抑制mTOR進而阻止因interleukin-2引起的淋巴球活化訊息傳導及細胞分裂。主要的副作用包含高血脂、貧血、蛋白尿、傷口不易癒合(移植術後不建議立即使用此類藥品)與腸胃道症狀等。雖然此類藥物沒有直接的腎毒性,卻可能因併用CNI類藥物,例如Sirolimus會與Cyclosporine的代謝物產生交互作用而出現腎毒性;因此Sirolimus最好單獨使用,或與類固醇或其他類抗增生藥物併用。
藥物劑量仍須依血中最低治療濃度(Trough Level)調整。Sirolimus建議的最低治療濃度是5-15 ng/mL,典型劑量為2-5 mg/day,單次給予;Everolimus建議最低治療濃度是3-8 ng/mL,典型劑量則為0.75-1.5 mg,每天兩次。
3. Inosine Monophosphate Dehydrogenase Inhibitors:
Azathioprine(安思平錠)、Mycophenolic acid(MPA,睦體康腸衣錠;MMF,山喜多╱喜妥善膠囊)。
Azathioprine為一種purine類藥物,經由肝臟代謝轉換成具藥理活性的6-mercaptopurine(6-MP),再由xanthine oxidase分解代謝。
Azathioprine主要抑制DNA合成進而抑制活性淋巴球的增殖。骨髓抑制是此藥物使用受限的主因,但通常是可逆的,只要將藥物劑量減低或暫停用藥即可。一般維持劑量是1.5-2.5 mg/kg/day,單次給予。Azathioprine和Allopurinol/Febuxostat為併用上的禁忌,以防止嚴重骨髓抑制的危險。
Mycophenolate mofetil(MMF)為前驅物,體內可被轉換為其活性代謝物mycophenolic acid(MPA)。MPA藉由阻斷inosine monophosphate dehydrogenase來阻斷細胞purine的de novo合成,可選擇性阻斷淋巴球的增生而不影響其他器官正常細胞。主要的副作用是腸胃不適(噁心、腹瀉、腹痛)與血液學障礙(白血球低下、血小板低下)。一般劑量為1-2 g/day,分次給予;但含有鎂與鋁的制酸劑會干擾MPA的吸收,不可與此藥同時給予。
生物抗體製劑
抗體製劑如多株抗體(兔抗胸腺細胞免疫球蛋白)或單株抗體(Basiliximab新睦樂、Rituximab莫須瘤、Eculizumab舒立瑞)因長期使用,可能增加移植後淋巴增生疾病或惡性腫瘤(特別是淋巴癌)的發生機率,因此多用於移植手術前後的誘導治療或治療急性排斥為主。
感染預防
1.移植前評估時即應給予肺炎鏈球菌及B肝疫苗的施打,但移植術前及術後則應避免活體疫苗。流感疫苗應每年施打,水痘疫苗在血清陰性及A型肝炎疫苗(尤其活體肝移植者)在移植前評估也都應被考慮。
2.術後第一個月內多以細菌感染引起肺炎、敗血症、泌尿道感染與傷口感染為多;念珠菌感染則常發生在使用廣效性抗生素有靜脈注射管線的患者。術後一個月至一到數年間,則以病毒感染或伺機性病原感染最常見。
巨細胞病毒(Cytomegalovirus,CMV)為台灣最常見病毒感染之一,受感染者多無明顯症狀,但終生潛伏並具傳染力;Ganciclovir(西美芬凍晶靜脈注射劑)或Valganciclovir(克毒癒膜衣錠)在移植術前CMV血清陽性或接受CMV血清陽性者的器官捐贈,即可用以預防CMV感染復發。
低劑量Baktar(撲菌特錠)可預防泌尿道感染、肺囊蟲肺炎感染;Fluconazole(泰復肯)或Voriconazole(黴飛)可預防或治療多數真菌感染,Posaconazole(波賽特)可用以預防器官移植的高危患者侵襲性麴菌與酵母菌的感染;Nystatin懸浮液則可預防口咽念珠菌的感染。

都是為了讓移植患者能獲得抗排斥藥物的最大效益,最小副作用,因此醫病溝通,藥師協助評估用藥合適性,都是必要的;此外,如讓民眾更認同器官捐贈,能有更多受贈機會,讓愛延續。
參考文獻:
1.華盛頓內科學手冊,第三十四版。
2.器官移植-發現問題.尋求答案,臺灣移植醫學學會。
3.藥物仿單。
4.中國醫藥大學附設醫院電子處方集。
5.電子醫學資料庫-UpToDate。
資料來源 : 中國醫訊第192期
